|

|
골수증식종양과 골수형성이상/골수증식종양의 진단 및 치료를 위한 이화여자대학교의과대학 진단검사의학과 박설희 배경
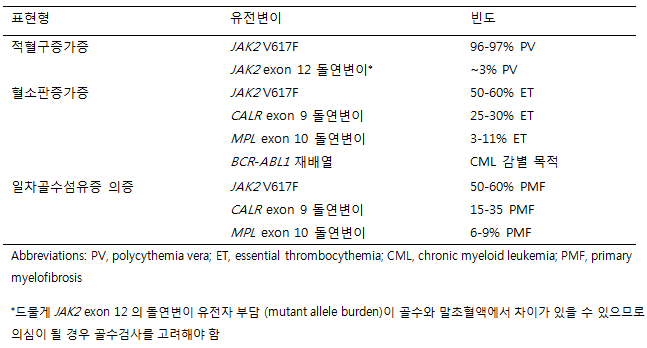
혈액질환 환자의 진단과 치료에서 유전학과 유전체학의 역할이 지속적으로 증대하고 있다. 차세대염기서열 (NGS) 패널이 널리 사용 가능해지면서 표준화된 접근법에 대한 논의를 통해 특정 검사의 적정한 사용에 대한 기준이 제시되고 있다. 여기에서는 WHO 분류에서 정의한 성인 만성골수종양 (chronic myeloid neoplasms) 의 유전학적 그리고 유전체학적 검사의 적용에 대해 2021년 영국혈액학회(British Society for Haematology)가 제시한 내용을 중심으로 살펴보고자 한다. 고전적 BCR-ABL1 음성 MPN (myeloproliferative neoplasm) 1. 적혈구증가증, 혈소판증가증, 골수섬유증 의증, 비전형적 혈전증의 스크리닝 검사 MPN의 분자 스크리닝 검사로 말초혈액의 DNA를 이용해 MPN 표현형 드라이버 돌연변이(JAK2, CALR, MPL)의 여부를 확인할 수 있다 (표 1). 이 검사로 대부분의 진성적혈구증가증 (polycythemia vera, PV) 환자와 본태혈소판증가증(essential thrombocythemia, ET), 일차골수섬유증(primary myelofibrosis, PMF) 환자의 85-90% 환자를 진단할 수 있어 순차적으로 하나씩 검사를 하거나 NGS 등의 방법으로 다중 PCR 검사를 할 수 있다. 검사소요시간과 민감도가 검사 방법을 결정하는 요소가 되는데 JAK2 V617F는 변이형 대립유전자 빈도(variant allele frequency, VAF) 1-3% 미만, JAK2 exon 12, CALR exon 9, MPL exon 10 변이형은 5% VAF 미만의 민감도가 요구되며, MPN이 의심되는 환자에서 광범위 골수성 NGS 패널은 지양된다. 표1. MPN이 의심되는 환자 대상 말초혈액 스크리닝 유전자검사
진단 시에는 돌연변이 유전자 부담의 보고가 필수적이지 않으나 질환의 진행 평가나 분자유전학적 반응 판정이 필요한 경우 등의 예외적인 상황이 있다. JAK2 V617F의 돌연변이 유전자 부담이 낮으면서(<1%) MPN 표현형을 보이는 경우에는 CALR과 MPL 돌연변이가 동시에 있을 수 있다. 만성골수백혈병(CML) 환자에서 티로신 키나제 억제제(tyrosine kinase inhibitor, TKI) 치료로 분자유전학적 반응이 좋음에도 불구하고 혈소판증가증 또는 다른 MPN의 특성이 관찰될 경우 JAK2 V617F, CALR 돌연변이 검사가 필요하다. JAK2 V617F 는 정상인에서도 발견되며 연령이 증가함에 따라 빈도가 증가하므로(clonal hematopoiesis of indeterminate potential, CHIP) 해석에 주의가 필요하다. 골수의 형태학적 이상이 발견되더라도 말초 혈액의 혈구 수가 정상인 경우엔 치료에 대한 근거가 부족하다.
2. 골수성유전자 패널 검사를 통한 추가적인 체세포 드라이버 돌연변이 검사와 세포유전학적 분석 MPN 환자에서 추가적으로 발견되는 체세포 드라이버 돌연변이인 TET2 (10-15%), ASXL1 (5-10%), DNMT3A (5-10%) 유전자의 소규모 변이는 CHIP과도 관련이 있다. MPN 환자에서 splicing, 염색질구조, 후성적기능(epigenetic functions), 신호전달(cellular signaling )과 관련한 돌연변이는 발견 빈도가 낮다. 이 같은 변이는PMF, post-PV MF, post-ET MF, MPN 또는 MDS/MPN의 모세포기에 발견 빈도가 높다. NGS 패널은 한꺼번에 골수성유전자를 검사할 수 있으며 일반적으로 5% VAF 이상의 변이를 보고하고 말초혈액보다는 골수검체를 선호하며 연령이 높은 환자의 경우 CHIP이 우연히 발견될 수 있음을 고려해야 한다. 고전적 세포유전학적 검사로 흔한 염색체 수적 이상이나 결손이 PMF, post-PV MF, post-ET MF 환자의 45% 정도에서 관찰되는데, 20q-, 13q-, +8, +9, 1q+, -7/7q-가 흔히 관찰된다. 광범위 NGS 패널 및 단일염기다형성(SNP) 어레이 검사는 해상능이 높지만 균형 전위는 식별하지 못하고 대신 copy-number-neutral loss of heterozygosity (CN-LOH)를 감지할 수 있다. 진단 시 비정상핵형이 ET 환자의 5-10%, PV 환자의 약 15%에서 보고되며, 이러한 소견이 어느 정도 예후적 의미를 가질 수 있지만 1차 치료가 달라지지는 않는다. 1) MPN이 의심되지만 스크리닝 검사에서 음성인 적혈구증가증 JAK2 V617F 돌연변이가 없는 적혈구증가증 환자에서 JAK2 exon 12 돌연변이 검사를 고려할 수 있으나 대부분은 특발성 적혈구증가증으로 진단된다. 이 경우 분자유전학적 병인은 밝혀지지 않았고, SH2B3 돌연변이가 보고된 경우는 적혈구조혈인자의 감소에 의한 적혈구증가증이었다. 특발성 적혈구증가증의 경우 유전자 패널 검사나 세포유전학적 검사를 권장할 근거가 부족하다. 2) 혈소판증가증 또는 PMF 의증 Triple-negative ET 또는 PMF 환자의 10-15% 에서 골수성유전자 패널 검사로 클론성을 증명할 수 있다. 단, 부수적CHIP의 가능성도 있으므로 이를 고려하여 판단한다. Triple-negative PMF 환자의 포괄적 게놈 분석의 절반이상에서 돌연변이가 발견되었고, 1/3에서는 비정상핵형을 가지고 있었다. 따라서 골수 조직 및 임상 양상이 PMF와 일치하는 환자의 경우 기존 염색체 검사(또는 SNP 어레이)와 함께 골수성유전자 패널 검사가 권장된다. Triple-negative ET의 진단은 조직학적 방법으로 이루어지는데, 80%이상에서 돌연변이나 염색체 이상이 발견되지 않았다. 다른 종류의 골수성유전자 돌연변이가 관찰될 경우엔 MDS/MPN을 포함한 감별진단이 필요하다. Triple-negative 혈소판증가증 환자에서는 광범위 골수성유전자 패널 검사의 근거가 부족하고, MPN 표현형 드라이버 유전자변이의 재검은 몇 년에 한 번 하는 정도가 적당하다. 일부 상황에서는 클론성의 증명을 위해 시행해 볼 수는 있다.
골수 조직학이 정상 또는 반응성을 보이는 환자의 경우엔 골수성유전자 패널과 세포유전학적 검사는 필요하지 않고, MDS나 MDS/MPN의 특성이 있는 경우에 필요하다.
3) JAK2, CALR 또는 MPL 돌연변이가 알려진 환자 추가적인 분자유전학적 정보를 통해 JAK2 V617F와 관련된 MDS/MPN 같은 질환을 진단할 수 있다.
추가적인 체세포 드라이버 돌연변이의 존재는 PMF, PV 및 ET에서 예후적 의미가 있다. 예후 스코어링 모델은 단일 유전자 정보, 포괄적인 게놈 및 세포유전학적/복제 수 프로필까지 다양한 방식의 분자유전학적 정보를 통합하여 제시한다 (표 2). 동종조혈모세포이식을 위해서는 정확한 예후 판정을 위해 골수성유전자 패널 검사와 기존 염색체 검사가 가장 유용하다. 예후 판정을 위한 검사는 모든 환자에서 고려할 수 있다. 표2. PMF, post-PV MF, post-ET MF의 예후 점수 시스템에서의 세포유전학적 정보와 분자유적학적 정보
3. 질병 모니터링: 클론 부담의 정량적 분석 현재 JAK2 V617F 돌연변이 대립유전자 부담의 정량적 분석은 공식적인 치료 목표의 근거로써 증명되지 않아 일반적인 모니터링 지표로 권고되지는 않는다. 고감도 정량적 분석을 사용한 평가는 저용량 페길화 인터페론 알파에 대한 혈액학적 반응이 있는 환자에서, 추가 용량 감소 또는 치료를 하지 않는 임상시험을 위해 연간 기준으로 해 볼 수는 있다. 잔존질환을 모니터링하고 임상 재발 전에 기증자-림프구 주입을 안내하기 위해 동종조혈모세포이식 후 환자에게 사용할 수 있다.
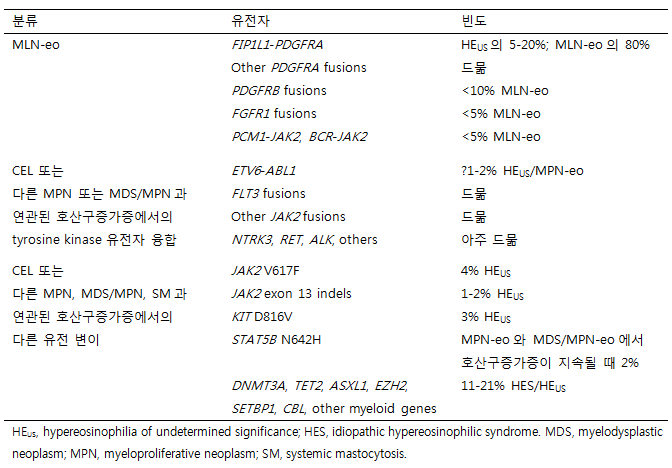
비정형 골수증식성 신생물 1. 만성호산구백혈병(chronic eosinophilic leukemia, CEL) 및 호산구증가증을 동반한 골수구계 및 림프구계 종양(myeloid/lymphoid neoplasms with eosinophilia, MLN- eo) 명백한 이차적 원인이 없는 최소 1.5×109/L의 지속적인 호산구증가증이 있는 환자는 FISH 또는 중첩 역전사효소 (nested RT-) PCR로 말초혈액 또는 골수에서 FIP1L1-PDGFRA에 대해 조사해야 한다. 그 외의 TK 유전자 재배열은 세포유전학적 검사를 통해 발견할 수 있으므로 골수로 검사하면 된다. 광범위 또는 타겟유전자 RNAseg 스크리닝 검사법으로 다양한 재배열유전자가 발견되었지만 현재까지는 비용대비 선별검사로서는 적합하지 않다. MLN-eo 의심 시PDGFRA, PDGFRB, FGFR1, JAK2를, CEL 의심 시 ABL1, FLT3, ETV6, 다른TK 유전자를 break-apart FISH 분석을 통해서도 식별할 수 있다. FIP1L1-PDGFRA를 포함한 융합유전자가 세포유전학적 또는 FISH 에 의해 발견되면 표적요법의 효과를 판정하기 위해 분자유전학적 방법으로 확인하는 것이 필요하다. 검사 시기는 CML에 권장되는 시기를 따른다. TK 유전자 융합이 없으면서 혈청 트립타제가 상승하는 경우 골수의 조직학 검사가 필수적이며 비만세포증을 고려해야 한다. 위의 표지자에 대해 음성이면 호산구증가증과 관련된 클론성을 증명하기 위한 다른 표지자가 포함된 골수성유전자 패널 분석을 고려해야 한다(표 3). 표3. 호산구증가증과 연관된 분자유전학적 이상
2. 만성호중구백혈병과 미분류 골수증식종양 CSF3R 돌연변이는 만성호중구백혈병(CNL)과 연관되지만 CNL에 국한되는 것은 아니다. CNL과 MDS/MPN 은 유전자 돌연변이 패턴에서 상당한 중첩을 보이며 이는 동일한 질환군임을 시사한다. ASXL1 돌연변이는 한 연구에서 CNL의 불리한 예후와 관련이 있었지만ruxolitinib에 대한 반응에는 영향을 미치지 않았다. 미분류골수증식종양 (MPN-U)는 대부분의 경우 JAK2 V617F, CALR 또는 기타 골수성 드라이버 돌연변이에 대해 양성 반응을 보인다.
골수이형성/골수증식성 종양 성인 MDS/MPN 중복 (overlap) 증후군의 진단은 골수 형태와 임상 평가에 크게 의존한다. 그러나 분자 유전학은 이러한 질환의 스펙트럼 전반에 걸쳐 진단, 하위 분류 및 예후에 관련한 핵심 정보를 제공할 수 있다. 1. 골수이형성/골수증식성 종양이 의심되는 환자의 초기 검사 MDS/MPN이 의심되는 환자는 초기에 BCR-ABL1 과 MLN-eo와 연관된 유전자재배열이 배제되어야 한다. 세포유전학은 클론성을 입증하고 예후를 제시하는 중요성 때문에 진단 시 수행해야 하며 MDS/MPN을 모방하는 드문 TK 재배열유전자를 확인하기 위해서도 필요하다. 30-50%에서 +8, +9, -7, 7q-, 20q-, 13q- 및 i(17q)의 세포유전학적 이상이 발견되고, +8, 염색체 7의 이상 또는 복합 핵형의 검출은 CMML에서 안 좋은 예후로 알려져 있다. 세포유전학적 샘플이 없거나 결과 보고가 어려운 경우, SNP 어레이 분석으로 비정상의 검출율을75%까지 높일 수 있다. 7번과 8번 염색체에 대한 FISH는 반드시 해야 한다.
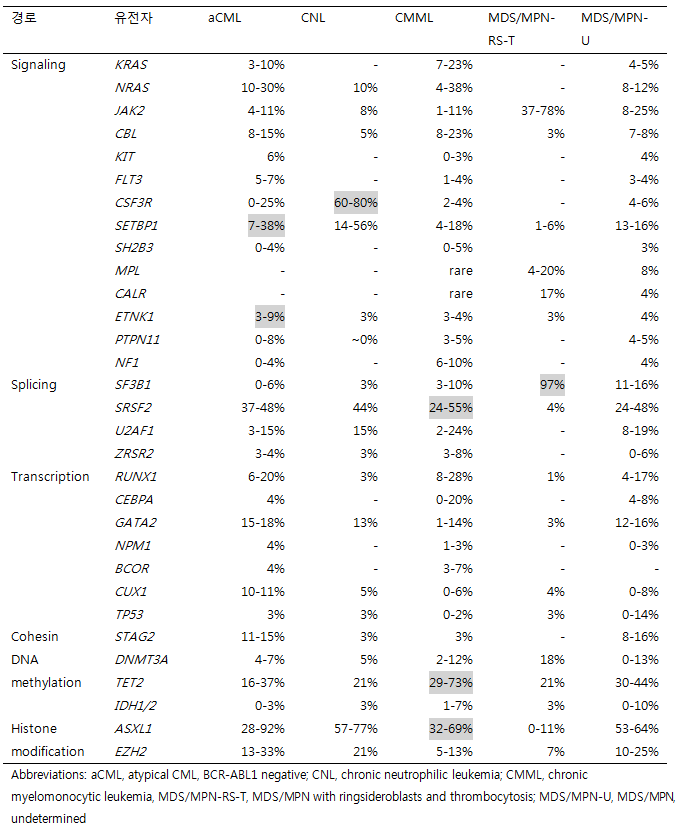
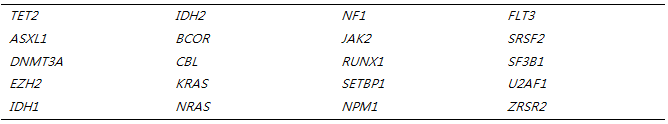
2. 골수성유전자 패널 검사를 통한 추가적인 체세포 드라이버 돌연변이 1) 미결정 조직학적 소견의 환자 체세포 돌연변이는 MDS/MPN 중복증후군환자의 90% 이상의 사례에서 발생하는 것으로 보고된다. 높은 빈도로 검출되는 체세포 돌연변이는 클론성의 근거도 되지만 연령이 높은 경우 건강인에서도 관찰된다는 점을 고려해야 한다. CMML의 가능성이 있는 환자에서 명확한 형태학적 특징이 없음에도 체세포 돌연변이가 있는 경우에 CMML 환자와 유사한 임상 표현형 및 유전자형을 보였으며 안 좋은 예후가 확인되었다. 따라서 골수성유전자 패널은 진단이 어려운 경우에 권장되며 돌연변이가 두 개(그 중 하나는 높은 VAF>20%)가 존재하면 진단을 뒷받침할 수 있다. MDS/MPN 중복증후군이 의심되는 경우 표4와 같은 체세포 돌연변이에 대한 조사가 필요하다. 표5는 CMML이 의심되는 환자에 최소한으로 권장되는 유전자이다. 표4. CNL과 MDS/MPN에서의 흔한 유전 변이
표5. CMML에서의 타겟 염기서열검사에 포함되어야 할 유전자
3. MDS/MPN 진단이 확인된 환자 MDS/MPN에서 일반적으로 발견되는 유전자 돌연변이는 한 질환에 특이적이지는 않지만 유전형/표현형 상관관계가 있어 하위 분류에 도움이 된다. 또한 예후와 관련된 유전자의 돌연변이는 치료제의 표적(JAK2, IDH1/2)이 될 수 있다. CMML과 관련하여 SRSF2, TET2 및 ASXL1돌연변이가 가장 일반적이며TET2돌연변이 + SRSF2 돌연변이 또는 TET2돌연변이+ ZRSR2의 돌연변이 조합은 CMML 표현형에 대해 매우 특이적이다. aCML의 진단은 SETBP1 및/또는 ETNK1의 돌연변이로 도움을 받을 수 있고, 이는 각각 25-38% 및 10% 정도에서 보고된다. SETBP1돌연변이는 CNL에서도 발견된다. MDS/MPN-RS-T에서 SF3B1 및 JAK2의 돌연변이가 최대 90% 및 57%에서 보고되며 15% 환상철적모구가 있고 SF3B1 돌연변이가 검출되면 진단이 가능하다. MDS/MPN에서 트립타제 증가 및/또는 비만 세포 이상은 관련 혈액신생물이 있는 전신성 비만세포증을 시사하며, KIT D816V 의 발견으로 진단이 가능하다. MDS/MPN이 진단된 환자에서 KIT D816V 의 검출되면 비만세포증에 동시에 이환 되었을 가능성을 두고 골수 형태를 검토해야 한다. CMML에서 돌연변이 분석은 질병에 대한 예후 점수 시스템(CMML-specific prognostic scoring system, CPSS-molecular)에 통합되었으며 4개의 유전자(ASXL1, NRAS, RUNX1 및 SETBP1) 돌연변이가 나쁜 예후와 독립적으로 연관이 있다. aCML에서 SETBP1 돌연변이는 진행된 임상 표현형 및 낮은 생존율과 관련이 있고, MDS/MPN-RS-T 환자에서 SETBP1 및 ASXL1돌연변이는 모두 낮은 생존율과 관련이 있다. 말초혈액과 골수에서 검출된 돌연변이는 일치된 결과를 보이고, 후속 진단에 대한 높은 양성예측도 및 높은 음성예측도를 보이므로 클론성 마커의 존재를 확인하거나 침습적 검사를 피하기 위해 고령 환자 또는 골수생검에 적합하지 않은 환자에서 옵션이 될 수 있다.
결론 골수증식종양 및 골수형성이상/골수증식종양의 진단은 검사법의 발달에도 여전히 어려운 점이 있다. NGS의 도입으로 혈액 질환과 관련된 다양한 골수성유전자 돌연변이가 발견되었지만 특정 유전자 돌연변이가 한 질환에 국한되지 않아 진단을 위해서는 임상적, 조직학적, 유전학적 정보를 통합해서 분석해야 한다. 추후 유전학적 정보가 축적되어 진단 및 치료를 위한 표준화된 기준이 제시되길 기대한다. REFERENCE
|
Copyright © The Korea Society for Laboratory Hematology. All Rights Reserved.
|