| 서자영 (가천의대길병원) |
| 1. 응고질환의 분자유전학적
검사의 적응증 |
| 유전성 응고질환 환자의 상당수는 응고검사 결과와 출혈 또는 혈전증의 기왕력, 가족력 청취
등을 통해 진단이 가능하다. 따라서 응고질환의 진단을 위해 일차적으로 유전검사를 시행하는 것은 권장되지 않는다. 그러나 아래와 같은
목적을 위해서 응고질환의 분자유전학적 확진이 필요하다. |
| (1) Mild or equivocal phenotype을 보이는 환자의 확진 |
응고인자 또는 응고억제인자의 감소 정도가 경하거나 응고검사 결과만으로는 감별 진단이 어려운
경우 유전 검사를 통한 확진이 가능하다. vWF와 혈소판 표면의 GP1b 수용체의 친화력이 증가되어 있는 제2B형 폰빌레브란트병(vWD)과
혈소판형vWD는 VWF 유전자와GP1BA 유전자 검사를 통해 감별할 수 있다. 제VIII응고인자가 경도로 감소되어 있는 경우
F8 유전자와 VWF 유전자 검사가 경증 혈우병 A와 제2N형 vWD의 감별 진단에 도움이 된다. |
| (2) 산전검사 및 보인자 진단 |
| 가족 내에 이환된 환자가 있고, 유전 검사로 확진된 경우 다른 가족 구성원에 대하여 targeted
mutation analysis를 시행한다. 보인자에서 응고인자 수치는 정상일 수 있으며, 특히 상염색체 열성으로 유전되는 경우
응고검사 결과만으로 보인자 여부를 판별하는 것이 매우 어렵다. 산모 또는 다른 가족 구성원이 disease-causing mutation을
보유한 것으로 확인되면 태아의 chorionic villi나 amniocyte DNA로 산전 검사를 할 수 있다 |
| (3) 치료 반응 예측 |
| 유전성 응고질환에서 특정 genotype은 치료 성적과 연관이 있다. 원인 유전자의 large
deletion mutation이 있는 혈우병과 제3형 vWD의 경우 치료 중 inhibitor 발생의 위험이 높은 것으로 알려져
있다. |
| 2. 유전성 응고질환의
분자유전학적 검사 |
| 현재 대부분의 응고질환의 분자유전학적 검사는 염기서열분석검사를 기반으로 한다. 염기서열분석은
주로 coding exon과 consensus splicing site를 대상으로 하며, promoter region을 추가로 검사하기도
한다. 염기서열분석검사는 대부분의 point mutation을 검출할 수 있지만, large deletion/duplication
mutation이나 deep intronic mutation은 검출할 수 없다. 유전성 응고질환의 mutation spectrum은
유전자마다 매우 다양하기 때문에, 전략적 접근이 필요하다. 각각의 유전자 돌연변이의 종류와 분포는 Human Mutation Database
(HGMD) 및 유전자별 locus-specific database에서 확인할 수 있다. |
| 3. 유전성 출혈질환의
분자유전학적 검사 |
(1) Hemophilia A (혈우병 A) |
- F8 유전자 돌연변이에 의해 발생하며 X염색체성 유전, 남성 5,000~10,000명 당
1명에서 발생
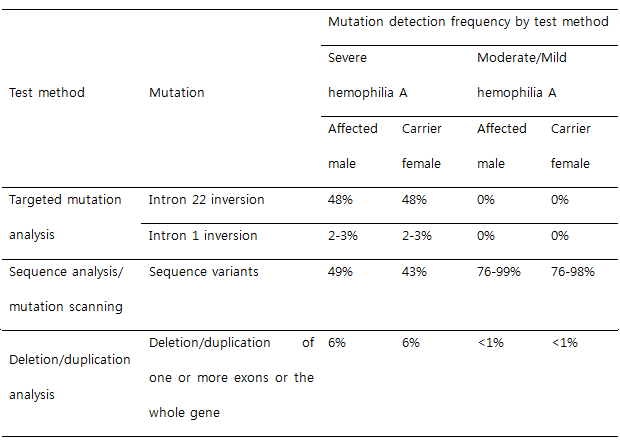
- 혈우병 A 환자의 F8 유전자 돌연변이 분포
|
 |
(fromhttp://www.ncbi.nlm.nih.gov/books/NBK1404/)
- Hemophilia A의 분자유전학적 진단 전략: F8은 26개의 exon으로 이루어진 크기가 186kb에 달하는 큰 유전자이므로,
질환의 중증도에 따라 분자유전학적 진단 strategy를 결정한다.
- Severe hemophilia A (FVIII activity <1%)
1단계: intron 22 inversion/intron 1 inversion mutation screening by long PCR
or inverse PCR
2단계: 1단계 검사에서 돌연변이가 검출되지 않으면 직접염기서열분석검사로 point mutation을 검사
3단계: 2단계 검사에서 돌연변이가 검출되지 않으면 multiplex ligation dependent probe amplification
(MLPA) 등의 방법으로 large deletion/duplication mutation을 검사
- Moderate/Mild hemophilia A (FVIII activity 1-5%/ 6-35%)
대부분 point mutation에 의해 발생하므로 염기서열분석검사를 1차로 시행하고, 돌연변이가 검출되지 않으면 intron inversion
또는 large deletion/duplication mutation에 대한 검사를 시행
- Validation of mutation: 관찰된 DNA change가 기존에 알려진 돌연변이인지를 검증하기 위해서 public
DB인 HGMD, HAMSTeRS (The Haemopohilia A Mutation, Structure, Test and Resource
Site, http://hadb.org.uk/) 등을 이용한다. Novel missense variation이 발견되면 가족 검사,
정상대조군 연구, functional study, bioinformatics 등을 이용한 검증이 필요하다.
- Inhibitor risk: 제VIII응고인자 replacement treatment를 받는 환자의 약 1/3에서 inhibitor가
발생하며, large deletion mutation에서 가장 risk가 큰 것으로 알려져 있다. Moderate/mild에서는
p.Arg612Cys, p.Arg2169His, p.Trp2248Cys 돌연변이를 가진 경우 inhibitor risk가 높은 것으로
보고되었다.
|
| (2) Hemophilia B (혈우병 B) |
- F9 유전자 돌연변이에 의해 발생하며 X염색체성 유전, 남성 25,000~30,000명
당 1명에서 발생
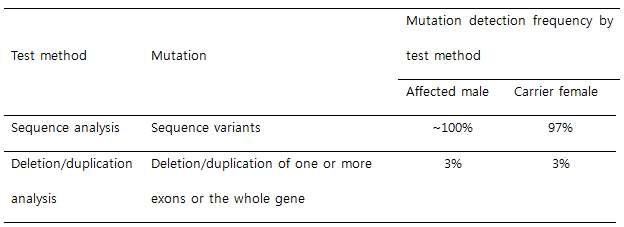
- Hemophilia B 환자의 F9 유전자 돌연변이 분포
|
 |
(fromhttp://www.ncbi.nlm.nih.gov/books/NBK1495/)
- Hemophilia B의 분자유전학적 진단: 대부분이 point mutation에 의해 발생하므로 염기서열분석검사를 1차로 시행하고
돌연변이가 검출되지 않으면 large deletion/duplication mutation에 대한 검사를 시행
- F8 mutation database: Factor IX Mutation Database (http://www.factorix.org/),
HGMD (http://www.hgmd.cf.ac.uk/)
|
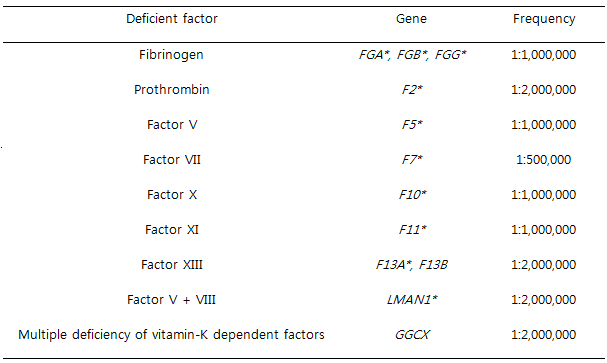
| (3) Rare autosomal recessive bleeding disorders |
- 전체 유전성 출혈 질환의 3~5%, 응고인자 검사에서 특정 인자의 결핍을 확인함
|
 |
| 4. 유전성 혈전증의 분자유전학적
검사 |
- SERPINC1 유전자 돌연변이에 의해 발생, 상염색체 우성 유전
- 돌연변이 분포: 항트롬빈 결핍 환자의 70~80%는 염기서열분석에서 돌연변이가 검출되고 약 10%는 large deletion
또는 duplication mutation을 가지고 있음
- 항트롬빈 결핍의 분자유전학적 진단: 1차로 SERPINC1 유전자에 대한 염기서열분석검사를 시행하고 돌연변이가 검출되지 않으면
large deletion/duplication mutation에 대한 검사를 시행
|
| (1) 항트롬빈 결핍(Antithrombin deficiency) |
- SERPINC1 유전자 돌연변이에 의해 발생, 상염색체 우성 유전
- 돌연변이 분포: 항트롬빈 결핍 환자의 70~80%는 염기서열분석에서 돌연변이가 검출되고 약 10%는 large deletion
또는 duplication mutation을 가지고 있음
- 항트롬빈 결핍의 분자유전학적 진단: 1차로 SERPINC1 유전자에 대한 염기서열분석검사를 시행하고 돌연변이가 검출되지 않으면
large deletion/duplication mutation에 대한 검사를 시행
|
| (2) C단백 결핍(Protein C deficiency) |
- PROC 유전자 돌연변이에 의해 발생, 상염색체 우성 유전
- 돌연변이 분포: C 단백 결핍은 거의 100% point mutation에 의해 발생함
- C 단백 결핍의 분자유전학적 진단: PROC 유전자에 대한 염기서열분석검사를 통해 유전성 C 단백 결핍 환자를 거의 100% 진단할
수 있으며, 유전성 C 단백 결핍이 강력하게 의심되나 PROC 유전자 염기서열분석검사에서 돌연변이가 나오지 않으면 large deletion/duplication
mutation 검사를 고려
|
| (3) S 단백 결핍(Protein S deficiency) |
- PROS1 유전자 돌연변이에 의해 발생, 상염색체 우성 유전
- S 단백 결핍의 분자유전학적 진단: 직접염기서열분석검사를 통한 PROS1 유전자 돌연변이 검출률은 약 50%에 불과한 것으로
알려져 있다. 유전성 S 단백 결핍증이 의심되는 환자의 PROS1 염기서열분석검사에서 돌연변이가 나오지 않으면 후속 검사로 MLPA를
이용한 large deletion/duplication mutation 검사를 시행하여 돌연변이를 확인해야 한다. 염기서열분석 및
MLPA 검사에서 모두 돌연변이가 관찰되지 않으면 RNA study나 promoter, regulatory region에 대한 검사를
시행해 볼 수 있다.
|
| (4) 플라스미노겐 결핍(Plasminogen deficiency) 또는 이상플라스미노겐혈증(Dysplasminogenemia) |
- PLG 유전자 돌연변이에 의해 발생, 상염색체 우성 유전
- 돌연변이 분포: 아시아인에서는 PLG유전자의 missense mutation으로서 dysplasminogenemia (type II plasminogen deficiency)를 유발하는 Ala620Thr (Ala601Thr)가 높은 빈도로 나타남
- 분자유전학적 진단: Plasminogen 결핍 또는 이상이 의심되면 먼저 PLG유전자의 Ala620Thr 돌연변이에 대한 targeted
mutation analysis를 시행한다. 일차 검사에서 돌연변이가 검출되지 않으면 PLG유전자의 전체 exon을 대상으로 염기서열분석검사를
시행한다. PLG유전자에는 pseudogene이 존재하므로 검사의 primer design 및 해석에 주의를 요한다.
|
| (5) Factor V Leiden & Prothrombin G20210A |
- 분자유전학적 진단: Factor V R506Q와 Prothrombin G20210A에 대하여
직접염기서열분석 또는 PCR-RFLP 시행
- Factor V Leiden과 Prothrombin G20210A는 Caucasian에서 유전성 혈전증의 가장 흔한 원인이지만
한국에서는 보고된 바가 없음
|
| 4. 참고문헌 |
- David Lillicrap.Molecular testing for disorders of hemostasis.Int
J Lab Hematol. 2013 Jun;35(3):290-6.
- UK Haemophilia Centre Doctors’ Organisation(UKHCDO). Practice Guidelines
for the Molecular Diagnosis of Haemophilia A.UPDATED July 2010. (http://www.cmgs.org/BPGs/best_practice_guidelines.htm)
- UK Haemophilia Centre Doctors’ Organisation(UKHCDO). Practice Guidelines
for the Molecular Diagnosis of HaemophiliaB.UPDATED December 2010. (http://www.cmgs.org/BPGs/best_practice_guidelines.htm)
- Pier MannuccioMannucci, Stefano Duga and Flora Peyvandi. Recessivelyinherited
coagulation disorders.Blood 2004 Sep 1;104(5):1243-52.
|

